助教または講師(助教級)を募集します。詳細は以下をご覧下さい。
公立大学法人
名古屋市立大学 大学院 医学研究科 教員公募
○募集分野
(募集部門) 神経発達・再生医学分野
○募集職位
助教または講師(助教級)(基準に満たない場合には採用を見送ることがあり
ます。
○募集人員 1 名
○採用予定日
令和 4 年 10 月1 日 以降の月の初日
○応募資格
① 博士学位を有する、あるいは着任までに取得見込みであること
② 神経発達・再生医学に関連した研究を行う意欲・能力を有すること
③ 研究室の学部生・大学院生等の研究指導を担当できること
④ 研究室の教職員と協力し研究室の運営に参加できること
⑤ 大学の運営・教育業務を担当できること
○選考方法
①応募書類 必要に応じて ②面接 を行い、これらを総合して決定
(応募者多数の場合は、応募書類による第 1 次選考を行います。)
面接を実施する場合は、追って通知します。
○給与等
公立大学法人名古屋市立大学職員の給与に関する規程 の定めるところによる
(初任給調整手当あり
任期制(5 年)再任可
裁量労働時間制
社会保険:公立学校共済組合
○応募方法
次の書類を、応募・問い合わせ先まで、郵送 または持参 してください。
①履歴書(指定様式)
② 業績目録 (指定様式
③今までの研究の概要( 1,000 字程度: A4 任意様式)
④志望動機と今後の抱負( 1,000 字程度: A4 任意様式
⑤現在照会できる方の連絡先2名
提出いただいた書類は採用審査の用途に限り使用され、選考終了後に適切に管
理・処分し、返却いたしませんので、ご了承ください。
○応募締切
令和 4 年 5 月 1 6 日( 月 )必着
○応募・問い合わせ先
〒 467-8601
名古屋市瑞穂区瑞穂町字川澄1番地
公立大学法人名古屋市立大学医学 ・病院管理部事務課 担当 伊藤・白野
TEL: 052(85 8 7107 E mail: jimuka_jimu@sec.nagoya cu.ac.jp
特任助教1名を募集します。詳細は以下をご覧下さい。
https://www.nagoya-cu.ac.jp/med/position/019749.html
[研究内容]
当研究室では、生後脳におけるニューロン新生機構について研究しております。また、脳疾患のモデル動物を用いて、神経幹細胞から産生されるニューロンが傷害部位へ移動・成熟して失われた脳機能を回復させるメカニズムを解析し、病態解明や新しい再生医療技術の開発につなげることを目指しています。
着任後は、主に新生児期におけるニューロン新生とその病態に関する研究をご担当いただきます。神経科学、細胞生物学、生化学、分子生物学のいずれかのバックグラウンドや、イメージング、scRNAseq、またはバイオインフォマティクス解析などの経験があれば研究遂行に役立つことが期待されますが、新しい分野にチャレンジする意欲があればご経験は問いません。
例えば、現在大学院最終学年の方、海外留学を予定していた方で新型コロナウイルスの影響で国内のポジションを探している方、海外で研究中で帰国したい方、なども歓迎いたします(詳細はお気軽に電話やメールでお尋ね下さい)。
[着任時期]
2021年4月1日以降できるだけ早期
*着任時期は相談に応じます。
<応募期限>
2020年12月18日(金)(必着)
※期限日前であっても、随時面接選考を行い、採用が決まり次第、公募を締め切ります。
[応募方法]
(1)履歴書(指定様式 *写真付、e-mailアドレスを必ず記載のこと)
(2)研究業績目録(形式自由)
(3)主な原著論文のPDF : 3編(業績が3編以下の場合は全て)
(4)これまでの業績の概要と習得している技術(形式自由)
(5)応募の理由と着任後の抱負(形式自由)
(6)照会可能な研究者2名/所属/連絡先
※全てメール添付にて送付してください。
[書類送付先]
神経発達・再生医学分野 筧理恵
E-mail:rie_k@med.nagoya-cu.ac.jp
[問い合わせ先]
神経発達・再生医学分野 澤本和延
TEL:052-853-8532
E-mail:sawamoto@med.nagoya-cu.ac.jp
[選考方法]
書類選考及び面接(WEBまたは対面)を行います。
金子准教授らの新しい論文がMolecular Brainに掲載され、ジャーナルのウェブページで紹介されました。
Kaneko N, Nakamura S, Sawamoto K
Effects of interferon-alpha on hippocampal neurogenesis and behavior in common marmosets.
Mol Brain 13: 98 (2020)
https://doi.org/10.1186/s13041-020-00639-9
This work has been featured on the journal web page.
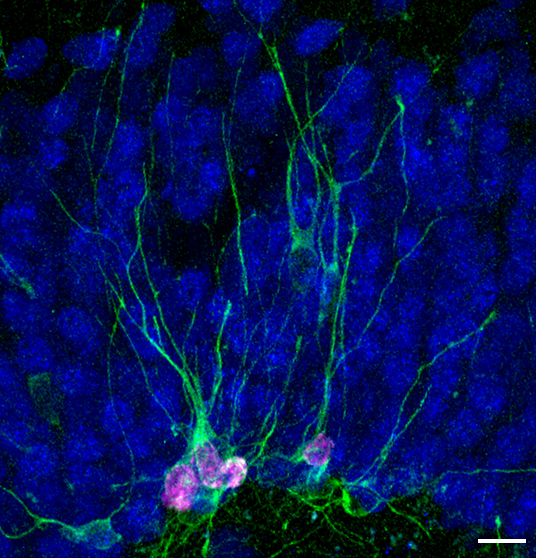
筆頭著者による研究内容の解説はこちら
大学院生のMariyam Akterさんと金子准教授らの新しい論文が、Cerebral Cortex誌に掲載されました。
Akter M, Kaneko N, Herranz-Perez V, Nakamura S, Oishi H, Garcia-Verdugo JM, Sawamoto K
Dynamic changes in the neurogenic potential in the ventricular-subventricular zone of common marmoset during postnatal brain development
Cerebral Cortex bhaa031
https://doi.org/10.1093/cercor/bhaa031
Article (free access):
https://academic.oup.com/cercor/advance-article/doi/10.1093/cercor/bhaa031/5763077?guestAccessKey=a2cb855e-19d3-4871-a660-630d3fed7da2
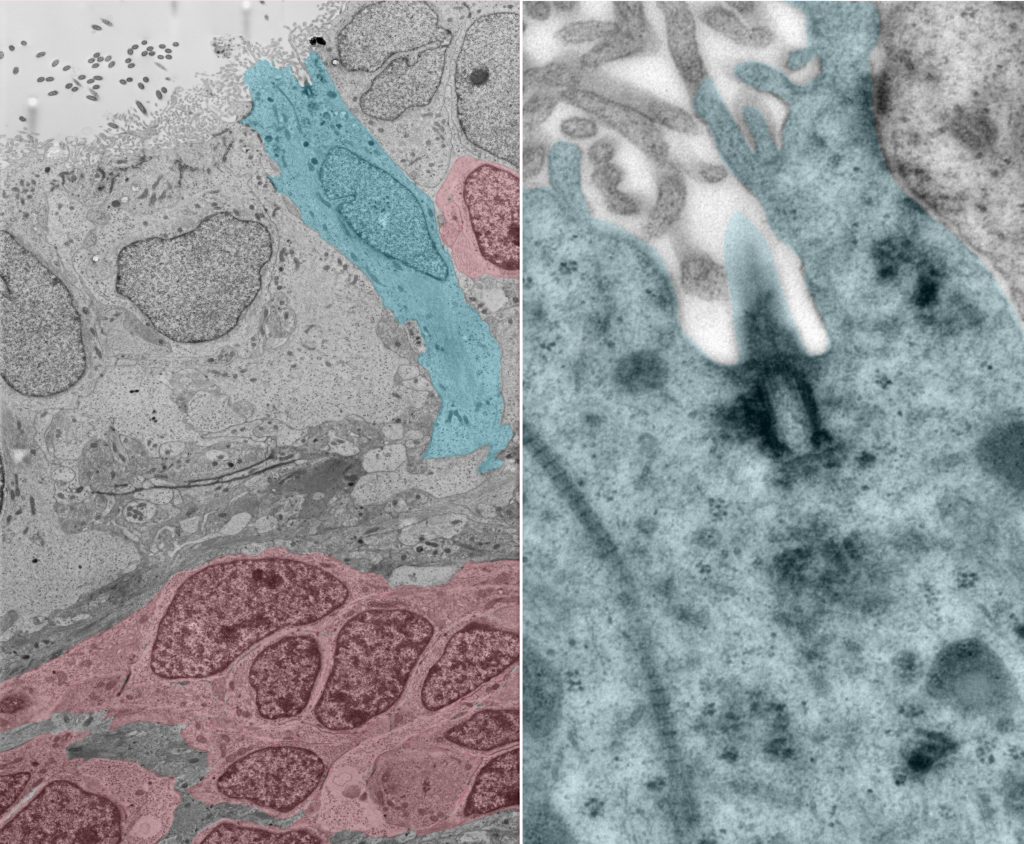
Electron microscopic images of the dorsolateral wall of the lateral ventricle in one-month-old common marmoset brain. (Left) A neural stem cell (cyan) and clusters of neuroblasts (red) are observed. (Right) Higher magnification view of the primary cilium of neural stem cell.
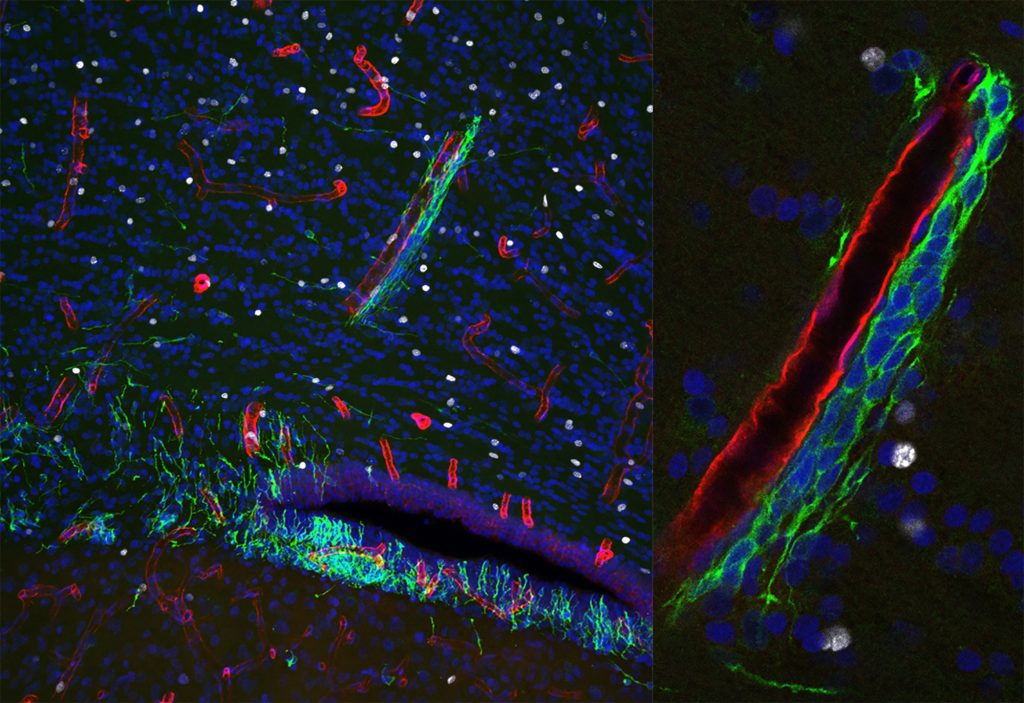
Immunohistochemistry of Dcx+ migrating neuroblasts (green) and CD31+ blood vessels (red) around the dorsolateral walls of the lateral ventricle in the six-month-old common marmoset injected with BrdU (white) during the first postnatal week. Nuclei are stained with Hoechst 33342 (blue). Right panel shows a higher magnification view of the chain-forming neuroblasts (green) migrating along the blood vessel (red) toward the developing neocortex.
大学院生の松本真実さんと澤田講師らの新しい論文がJ Neurosciに掲載され、本論文のデザインが表紙に採用されました。
Matsumoto M, Sawada M, García-González D, Herranz-Pérez V, OginoT, Nguyen HB, Thai TQ, Narita K, Kumamoto N, Ugawa S, Saito Y, Takeda S, Kaneko N, Khodosevich K, Monyer H, García-Verdugo JM, Ohno N, Sawamoto K
Dynamic changes in ultrastructure of the primary cilium in migrating neuroblasts in the postnatal brain.
J Neurosci 39: 9967-9988 (2019)
DOI: https://doi.org/10.1523/JNEUROSCI.1503-19.2019
This work has been featured on the journal cover.

新生ニューロンの三次元モデル 3D interactive modeling of migrating neuroblasts
Swelling-formation phase by Sawamoto Lab Data on Sketchfab
筆頭著者による研究内容の解説はこちら
名古屋市立大学大学院医学研究科神経発達・再生医学分野(名古屋市瑞穂区)では、生後脳におけるニューロン新生機構、特に新生ニューロンの移動メカニズムについて研究しております。また、脳疾患のモデル動物を用いて、神経幹細胞から産生されるニューロンが傷害部位へ移動・成熟して失われた脳機能を回復させるメカニズムを解明し、新しい再生医療技術の開発につなげることを目指しています。着任後は、脳傷害モデルにおけるニューロンの再生に関する新しい研究プロジェクトを担当していただきます(詳細は電話やメールでお尋ね下さい)。
[勤務地住所等]
〒467-8601
名古屋市瑞穂区瑞穂町字川澄1
名古屋市立大学大学院医学研究科
脳神経科学研究所
神経発達・再生医学分野
[募集人員(職名・採用人数等)]
特任助教 若干名
[募集期間] 2019年10月16日 ~ 2019年12月20日 必着
※ただし、期限日前であっても採用が決まった場合には、公募を締め切ることがあります。
[着任時期]
2020年4月1日着任予定
*着任時期は相談に応じます。2020年1月以降、4月までに着任いただける方を望みます。
詳細は、以下をご参照下さい。
https://jrecin.jst.go.jp/seek/SeekJorDetail?fn=3&id=D119101031&ln_jor=0
本募集は終了しました。ご応募ありがとうございました。
名古屋市立大学大学院医学研究科再生医学分野(名古屋市瑞穂区)では、生後脳におけるニューロン新生機構、特に新生ニューロンの移動メカニズムについて研究しております。また、脳疾患のモデル動物を用いて、神経幹細胞から産生されるニューロンが傷害部位へ移動・成熟して失われた脳機能を回復させるメカニズムを解明し、新しい再生医療技術の開発につなげることを目指しています。着任後は、脳細胞のシングルセル解析や、人工足場による再生促進効果の解析などに携わって頂く予定です(詳細はメールでお尋ね下さい)。
[勤務地住所等]
名古屋市瑞穂区瑞穂町川澄1
名古屋市立大学大学院医学研究科再生医学分野
[募集人員]
特任助教 1名
[着任時期]
2019年4月1日以降
*着任時期は相談に応じますが、10月までに着任いただける方で、早期に着任いただける方を望みます。
[応募書類送付先]
筧理恵
E-mail:rie_k@med.nagoya-cu.ac.jp
[問い合わせ先]
澤本和延
E-mail:sawamoto@med.nagoya-cu.ac.jp
2019年03月29日 ~
2019年04月30日 必着
ただし、期限日前であっても採用が決まった場合には、公募を締め切ることがあります。
詳細は下記リンク(JREC-INの公募ページへ移動します)をご確認ください。
https://jrecin.jst.go.jp/seek/SeekJorDetail?fn=3&id=D119031413&ln_jor=0
本募集は終了しました。ご応募ありがとうございました。
| 仕事内容 | マウスの行動解析、脳の組織解析、遺伝子改変マウスの繁殖管理、遺伝子タイピングなど。詳細はお問い合わせください。 |
| 雇用期間 | 平成31年7月1日〜平成32年3月31日まで 更新あり、応相談 |
| 勤務地 | 名古屋市瑞穂区瑞穂町字川澄1番地 名古屋市立大学大学院医学研究科 再生医学分野 |
| 給与等 | 時給:1,027円 ※応募資格:理系の大学、短大、専門学校卒、動物アレルギーのない方。未経験の方も指導いたします。 |
| 交通費 | 規程により支給。(上限850円) |
| 社会保険等 | 労災保険に規程により加入。 |
| 勤務日 | 月曜〜金曜のうち2日(国民の祝日は除く) ※勤務日は応相談。 |
| 勤務時間 | 午前10時00分〜午後3時00分まで(休憩1時間) ※勤務時間について相談可 |
| 募集人員 | 1名 |
| 応募方法 | 面接選考を行いますので、下記連絡先まで履歴書(書式自由・写真貼付)を郵送にて送付ください。2月22日(金)必着(面接の日時は追ってご連絡致します。) 但し、期間中でも採用者が決定次第終了。 |
| 問い合わせ及び担当者 | 〒467-8601 名古屋市瑞穂区瑞穂町字川澄1番地 名古屋市立大学大学院医学研究科 再生医学分野 担当:筧理恵 電話:052-853-8532 e-mail:rie_k@med.nagoya-cu.ac.jp |
脳梗塞は、脳血管の閉塞により血流が途絶して神経細胞が死滅する疾患で、それによって生じる様々な神経機能の障害は、現在我が国でも多くの人々を苦しめています。発症直後で脳が深刻なダメージを受けていない期間に行う、閉塞した血管を再開通させる治療法は、近年目覚ましく発達しました。しかし、成熟した脳では神経細胞を再生する能力がほとんどないため、この時期を過ぎると抜本的な治療法がないのが現状です。
この度、名古屋市立大学大学院医学研究科の澤本和延教授(再生医学)(自然科学研究機構生理学研究所 客員教授)・金子奈穂子准教授(再生医学)らは、自然科学研究機構生理学研究所・バレンシア大学・自治医科大学等の研究者と共同で、マウスを用いた実験により、脳内で新たに産生された神経細胞の傷害部への移動を促進することにより、脳梗塞後の神経機能が回復することを発見しました。
成熟した脳内では、特定の領域だけで少数の神経細胞が作られています。幼若な神経細胞は、脳内を遠くまで移動することができ、脳梗塞後には傷害部に向かって移動して脳を再生しようとしますが、ダメージを受けた脳組織内では神経細胞は十分に移動することができません。研究グループは、神経細胞がダメージを受けた組織内を移動するのに必要なタンパク質を同定して、このタンパク質の産生を増加させることにより、神経細胞の傷害部への移動が促進されることを発見しました。更に、傷害部の近くに再生する神経細胞を増やすことで、運動機能を回復させることに成功しました。
再生する神経細胞の配置を制御することが脳機能の回復に重要であることを示したこの研究成果は、脳梗塞やその他の脳傷害に対する再生医療の樹立に向けて重要なものです。
金子准教授らの新しい論文がScience Advances誌に掲載されました。
Kaneko N, Herranz-Pérez V, Otsuka T, Sano H, Ohno N, Omata T, Nguyen HB, Thai TQ, Nambu A, Kawaguchi Y, García-Verdugo JM, Sawamoto K.
New neurons use Slit-Robo signaling to migrate through the glial meshwork and approach a lesion for functional regeneration
Sci Adv 4: eaav0618 (2018)
脳梗塞は、脳血管の閉塞により血流が途絶して神経細胞が死滅する疾患で、様々な神経機能の障害が生じます。まだ脳が深刻なダメージを受けていない急性期に、閉塞した血管を再開通させる治療法は、近年目覚ましく発達しました。しかし、成熟した脳では神経細胞を再生する能力がほとんどないため、この時期を過ぎると抜本的な治療法がないのが現状で、我が国で、寝たきりの原因となる主な疾患のひとつです。神経細胞の大部分は胎生期に幹細胞からつくられますが、成熟過程でほとんどの幹細胞は消失します。そのため、成熟後の脳内では、脳室の周囲にある「脳室下帯」などごく限られた領域でしか神経細胞が作られません。脳室下帯で生まれた未熟な神経細胞は、脳梗塞後には傷害部に向かって移動して成熟し、神経細胞を再生しようとしますが、神経機能の障害を十分に回復させることはできません。本研究では、三次元的な電子顕微鏡解析法や、脳梗塞後の脳切片を移動する生きた神経細胞の挙動を記録するライブイメージングという方法で、ダメージを受けた脳組織で活性化して増殖・肥大化するアストロサイトと呼ばれる細胞が、神経細胞の移動を妨げていることを発見しました。
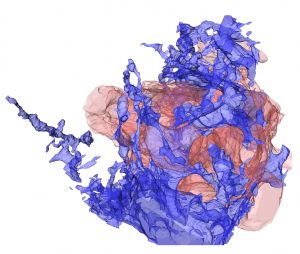 また、神経細胞が活性化アストロサイトの間をスムーズにすり抜けるのに必要なスリットという蛋白質を同定しました。神経細胞が分泌したスリットが、活性化アストロサイトの細胞表面にあるロボというタンパク質(受容体)に結合すると、細胞の骨組みをつくる蛋白質の動態が変化して活性化アストロサイトの形が変わり、神経細胞がすり抜けやすくなります。しかし、スリット蛋白質は、傷害部への移動の途中で減少していくため、神経細胞は十分に移動することができません。そこで、神経細胞のスリット蛋白質の産生を増加させる処置を行うと、脳梗塞後の脳組織内での神経細胞の移動を促進することができました。その結果、傷害部の近くまで移動して成熟する神経細胞の割合が増加し、それに伴って脳梗塞によって生じた運動機能の障害が改善しました。この研究から、損傷後の脳内で、新しい神経細胞の移動をコントロールして適切な場所に配置することが、脳機能の再生に重要であるということが分かりました。この研究で明らかになった脳の再生の仕組みは、脳疾患に対する再生医療の実現に向けても重要なものです。
また、神経細胞が活性化アストロサイトの間をスムーズにすり抜けるのに必要なスリットという蛋白質を同定しました。神経細胞が分泌したスリットが、活性化アストロサイトの細胞表面にあるロボというタンパク質(受容体)に結合すると、細胞の骨組みをつくる蛋白質の動態が変化して活性化アストロサイトの形が変わり、神経細胞がすり抜けやすくなります。しかし、スリット蛋白質は、傷害部への移動の途中で減少していくため、神経細胞は十分に移動することができません。そこで、神経細胞のスリット蛋白質の産生を増加させる処置を行うと、脳梗塞後の脳組織内での神経細胞の移動を促進することができました。その結果、傷害部の近くまで移動して成熟する神経細胞の割合が増加し、それに伴って脳梗塞によって生じた運動機能の障害が改善しました。この研究から、損傷後の脳内で、新しい神経細胞の移動をコントロールして適切な場所に配置することが、脳機能の再生に重要であるということが分かりました。この研究で明らかになった脳の再生の仕組みは、脳疾患に対する再生医療の実現に向けても重要なものです。
Stroke is a leading cause of death and chronic disability in adults, causing a heavy social and economic burden worldwide. However, no treatments exist to restore the neuronal circuitry after a stroke. While most neurons are generated during embryonic brain development, new neurons continue to be produced in the ventricular-subventricular zone (V-SVZ) of the adult brain. In rodent olfaction, immature new neurons called neuroblasts form chain-like aggregates that migrate to the olfactory bulb, where they differentiate into interneurons. However, in the case of brain injury, the mammalian brain has only a limited ability to regenerate neuronal circuits for functional recovery. In a rodent ischemic stroke model induced by transiently blocking the middle cerebral artery, the most commonly affected vessel in human patients, some V-SVZ-derived neuroblasts migrate toward the lesion, where they mature and become integrated into the neuronal circuitry. However, the number of these new neurons is insufficient to restore neuronal function.
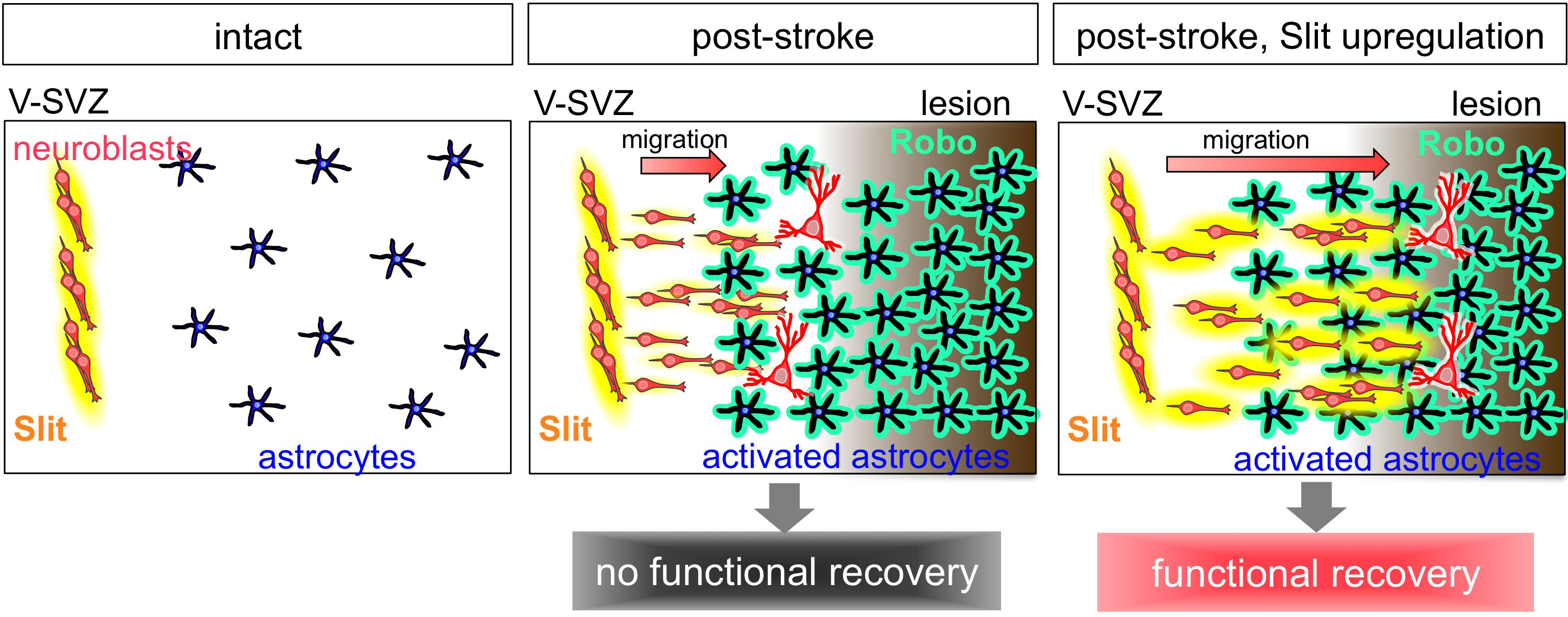
We have revealed a novel mechanism for neuronal regeneration, using the mouse model for ischemic stroke. Within a few days after stroke, astrocytes, a major population of macroglia, in and around the injured area become activated, exhibiting larger cell bodies, thicker processes, and proliferative behavior. The migrating neuroblasts must navigate through this astrocyte meshwork to reach the lesion. Using three-dimensional electron microscopy and live imaging, the research team demonstrated that neuroblast migration is restricted by the activated astrocytes in and around the lesion. In normal, olfaction-related migration, neuroblasts secrete a protein called Slit, which binds to a receptor called Robo expressed on astrocytes. Slit alters the morphology of activated astrocytes at the site of neuroblast contact, to move the astrocyte surface away and clear the neuroblast’s migratory path. However, in the case of brain injury, the migrating neuroblasts actually down-regulated their Slit production, crippling their ability to reach the lesion for functional regeneration. Notably, overproducing Slit in the neuroblasts enabled them to migrate closer to the lesion, where they matured and regenerated neuronal circuits, leading to functional recovery in the post-stroke mice. These results suggest that strategies designed to help migrating neurons reach the lesion may improve stem/progenitor cell-based therapies for brain injury.

筆頭著者による研究内容の解説はこちら
生理学研究所研究会「神経発達・再生研究会」が、名古屋市立大学病院大ホールで開催されました。
生理学研究所では、新分野の創成を目指す研究討論会として、様々なテーマの「生理研研究会」を、原則として自然科学研究機構岡崎地区において開催しております。この度、2018年度の生理研研究会の1つを、「神経発達・再生研究会」と題しまして、名古屋市立大学において開催することになりましたので御案内いたします。
脳・脊髄や末梢神経系の発達・再生のメカニズムに関する最新の研究成果をご発表いただき、議論したいと思います。皆様のご参加をお待ちしております。
日 時:2018年10月17日(水) 13時開始 18日(木) 16時終了(予定)
会 場:名古屋市立大学病院 大ホール
参加費:無料
懇親会:一般 5000円、 学生/大学院生 3000円
研究会の詳細は、以下の研究会ホームページをご覧ください。
http://www.nips.ac.jp/dcs/nervews/
参加申込:9月28日(金)までに以下のサイトからお願い致します。http://www.nips.ac.jp/dcs/nervews/index.html
代表者:澤本和延(名古屋市立大学・生理学研究所)
世話人:古瀬幹夫(生理学研究所)
事務局:名古屋市立大学大学院医学研究科再生医学分野 金子奈穂子
E-mail: naokokaneko0504@gmail.com
ご不明な点がございましたら、お気軽に事務局までお問い合わせください。
【プログラム(予定)】
10/17 (1日目) 13:00-18:00
大塚俊之 京都大学ウイルス・再生医科学研究所
「神経幹細胞制御による脳形態形成の改変」
河崎洋志 金沢大学大学院医薬保健学総合研究科
「フェレットを用いた大脳皮質形成機構の解析」
太田訓正 熊本大学大学院生命科学研究部
「Tsukushiを介した神経幹細胞ニッチ制御と水頭症の連関」
中島欽一 九州大学医学研究院
「転写因子ND1によるミクログリアからニューロンへの直接分化転換機能」
榎本秀樹 神戸大学大学院医学研究科
「シュワン細胞に内包された神経分化能とその可塑性」
岡野栄之 慶應義塾大学医学部
「幹細胞システムを用いた神経系の再生医療と病態解析研究」
廣田ゆき 慶應義塾大学医学部
「大脳皮質発生におけるリーリンシグナルの機能」
澤本和延 名古屋市立大学大学院医学研究科
「脳の発達・再生における新生ニューロンの移動」
岡田誠治 九州大学医学研究院
「グリア瘢痕制御による中枢神経の再生」
10/18 (2日目) 9:00-16:00
五十嵐道弘 新潟大学大学院医歯学総合研究科
「哺乳動物成長円錐の分子基盤をどう理解するか?」
藤島和人 京都大学高等研究院iCeMS
「小脳回路における軸索束依存的な樹状突起形成メカニズム」
生沼泉 兵庫県立大学理学部
「神経発達を担うアクチン足場蛋白質の選択的スプライシングの時空間制御」
竹居光太郎 横浜市立大学大学院生命医科学研究科
「神経回路形成因子LOTUSによる脳内環境制御:神経再生医療技術への展開」
山下俊英 大阪大学大学院医学系研究科
「中枢神経障害と神経—生体システム連関」
高橋淳 京都大学iPS細胞研究所
「iPS細胞を用いたパーキンソン病治療」
東海地区の研究者によるショートトーク
石田章真 名古屋市立大学
荻野ひまり 名古屋市立大学
桐生寿美子 名古屋大学
笹倉寛之 愛知医科大学
足澤悦子 生理学研究所・大阪大学
鳴島円 生理学研究所
丹羽智史 愛知医科大学
浜田奈々子 愛知県コロニー発達障害研究所
藤掛大学院生・澤田助教らの新しい論文がJournal of Neuroscienceに掲載されました。
Fujikake K, Sawada M, Hikita T, Seto Y, Kaneko N, Herranz-Pérez V, Dohi N, Homma N, Osaga S, Yanagawa Y, Akaike T, García-Verdugo JM, Hattori M, Sobue K, Sawamoto K
Detachment of chain-forming new neurons by Fyn-mediated control of cell-cell adhesion in the postnatal brain.
J Neurosci 38: 4598-4609 (2018)
https://doi.org/10.1523/JNEUROSCI.1960-17.2018
This work has been featured on the journal cover

筆頭著者による研究内容の解説はこちら
新しいメンバーが参加しました。New members have joined our lab.
澤田雅人助教らの新しい論文がEMBO Journalに掲載されました。
Sawada M, Ohno N, Kawaguchi M, Huang S, Hikita T, Sakurai Y, Nguyen HB, Thai TQ, Ishido Y, Yoshida Y, Nakagawa H, Uemura A, Sawamoto K
PlexinD1 signaling controls morphological changes and migration termination in newborn neurons
EMBO J 37: e97404 (2018)
http://emboj.embopress.org/cgi/doi/10.15252/embj.201797404
This work has been featured on the cover of the second February issue of the EMBO Journal

筆頭著者による研究内容の解説はこちら
韓国・漢陽大学医学部1年生 権さんの歓迎会をしました。
Welcome dinner for Mr. Inbeom KWON, a first year student at Hanyang University Medical School.


神農英雄研究員(新生児・小児医学分野)らの論文がCell Stem Cellに掲載されました。
Jinnou H, Sawada M, Kawase K, Kaneko N, Herranz-Pérez V, Miyamoto T, Kawaue T, Miyata T, Tabata Y, Akaike T, García-Verdugo JM, Ajioka I, Saitoh S, Sawamoto K
Radial glial fibers promote neuronal migration and functional recovery after neonatal brain injury.
Cell Stem Cell 22: 128-137 (2018)
https://doi.org/10.1016/j.stem.2017.11.005
This paper is now featured on the cover of the January 2018 issue of Cell Stem Cell



筆頭著者による研究内容の解説はこちら
周産期医療の進歩により新生児の生存率は劇的に改善しましたが、重篤な神経学的後遺症を高率に合併する、低酸素性虚血性脳症などの新生児脳障害は依然として毎年数千人程度発生しています。傷害で失われた神経細胞(ニューロン)を再生させる治療法は未だ無いのが現状であり、新たな治療法の開発が望まれています。
この度、名古屋市立大学大学院医学研究科の 澤本和延教授(再生医学)(自然科学研究機構生理学研究所を兼任)と、神農英雄研究員(新生児・小児医学)らは、東京医科歯科大学やスペイン・バレンシア大学などとの共同研究により、マウスを用いた実験で、新生児期のみに存在する脳障害後の神経再生メカニズムを世界で初めて発見しました。
「放射状グリア」という、脳の発生期に幹細胞としてはたらき、ニューロンの移動の足場となる細胞は、生後すぐに消失します。研究グループは、新生児期では脳障害後にこの放射状グリアが維持され、脳内に存在する幹細胞から産生されたニューロンが、放射状グリアの長い突起を足場として傷害部へ効率よく移動することを発見しました。さらに、放射状グリアを人工的に模倣した足場を新生児期の傷害脳へ埋め込むことによって、傷害部へのニューロンの移動を促進するとともに、歩行機能を回復させることに成功しました。
新生児期にのみ備わるこの神経再生メカニズムをヒトへ応用することによって、新生児脳障害の再生医療につながることが期待できます。

日時:2017年9月30日(土)13:00〜20:30
2017年10月1日(日)9:00〜13:00
会場:名古屋市立大学大学院医学研究科(桜山キャンパス)研究棟11階 講義室A
プログラム概要
◯ 2017年9月30日(土)
一般演題:8演題(予定)
特別講演:中島 欽一(九州大学大学院医学研究院応用幹細胞医科学部門)
教育講演:道川 誠(名古屋市立大学医学研究科病態生化学分野)
◯ 2017年10月1日(日)
一般演題:4演題(予定)
特別講演:池谷 裕二(東京大学大学院薬学系研究科薬品作用学)
教育講演:山嶋 哲盛(金沢大学医学系研究科/有松医科歯科クリニック)
世話人:名古屋市立大学大学院医学研究科再生医学分野 澤本和延
幹事:山嶋 哲盛(金沢大学/有松医科歯科クリニック)
原 英彰 (岐阜薬科大学薬効解析学研究室)
田村 了以(富山大学大学院医学薬学研究部(医学)統合神経科学)
櫻井 芳雄(同志社大学脳科学研究科)
事務局:名古屋市立大学大学院医学研究科再生医学分野
金子奈穂子・澤田雅人
仕事内容 マウスの行動解析、脳の組織解析、遺伝子改変マウスの繁殖 管理、遺伝子タイピングなど。詳細はお問い合わせください。
雇用期間 平成 29 年 4 月1日〜平成 30 年 3 月 31 日まで(年度更新制) 応相談 試用期間:1ヶ月
勤務地 名古屋市瑞穂区瑞穂町字川澄1番地 名古屋市立大学大学院医学研究科 再生医学分野
給与等 時給:1027〜1380 円(経験、資格に応じて名市大職員規程 に準じ処遇します。)
※応募資格 理系の大学、短大、専門学校卒、動物アレルギ ーのない方。未経験の方も指導いたします。
交通費 規程により支給。 社会保険等 健康保険・雇用保険・厚生年金保険・労災保険に規程により 加入。
勤務日 月曜〜金曜のうち 3〜5 日(国民の祝日は除く) ※勤務日は応相談。規程により有給休暇あり
勤務時間 午前 9 時 00 分〜午後 5 時 00 分まで(休憩 1 時間) ※勤務時間について相談可
募集人員 1 名
応募方法 面接選考を行いますので、下記連絡先まで履歴書(書式自 由・写真貼付)を郵送にて送付ください。
3 月 10 日(金)必着(面接の日時は追ってご連絡致します。) 但し、期間中でも採用者が決定次第終了。
問い合わせ及び 担当者 〒467-8601 名古屋市瑞穂区瑞穂町字川澄1番地 名古屋市立大学大学院医学研究科 再生医学分野 担当:西川みづ江 電話:052-853-8532 e-mail:mizue@med.nagoya-cu.ac.jp
研究室で忘年会をしました。良いお年をお迎え下さい。
We had an end of year party in the lab. I wish you a Happy New Year.
バレンシア大学を訪問し共同研究の打ち合わせをしました。
We visited University of Valencia and discussed our collaborative projects.


第1回研究室旅行として、鳥羽・伊勢へ行きました。We went to Toba and Ise as a lab trip.


第11回成体脳のニューロン新生懇談会を名古屋市立大学で開催しました。ご協力ありがとうございました。
The 11th Adult Neurogenesis Conference was held in Nagoya City University on November 14, 2015.
82名の方々にご参加いただきました。成体ニューロン新生と関連分野に関する特別招待講演1演題、口頭発表6演題、ポスター発表36演題と活発な討論が行われ、楽しい会になりました。当日のプログラムはこちらからダウンロードできます。
成体脳のニューロン新生懇談会ホームページはこちらです。来年は滋賀医大で開催される予定です。
参加には入会が必要です(会費無料)。ご希望の方は澤本までご連絡下さい。
バングラデシュからMariyam Akterさんが大学院生として入学しました。
Mariyam Akter from Bangladesh has joined our laboratory as a PhD course student
第58回日本神経化学会大会において、大学院修士課程の荻野崇君が優秀発表賞を受賞しました。
第11回成体脳のニューロン新生懇談会
発生期を終えた脳でも、海馬や側脳室周囲にある脳室下帯では、ニューロンが産生され続けています。近年の研究により、これらの領域で新生したニューロンは、神経の可塑性や再生に関与する、非常に興味深い役割を果たしていることが分かってきました。この会は、未発表なデータも含めた活発なディスカッションができるクローズドな懇談会として、10年以上前から毎年開催されてきました。
本年は、名古屋市立大学で懇談会を開催することになりました。「成体脳のニューロン新生」に加え、再生・発生・グリア新生などの関連分野を研究している方々にもご参加・ご発表頂き、交流を深める会になることを願っております。是非ご参加ください。
開催日:2015年11月14日(土)13:00〜
(受付:12:30〜)
会場:名古屋市立大学大学院医学研究科研究棟11階 講義室A
特別講演:向山 洋介 (Laboratory of Stem Cell and Neuro-Vascular Biology, National Heart, Lung, and Blood Institute, National Institutes of Health)
「神経幹細胞と成体ニューロン新生を支持する血管ニッチ」
演題募集:2015年7月1日〜2015年8月31日
参加登録:2015年11月10日まで
発表を希望される方は、参加・演題申込用紙に必要事項を記入し、事務局(naokoka@med.nagoya-cu.ac.jp)までお送りください。
会の詳細なご案内はこちらからダウンロードできます。
参加・演題申込用紙はこちらからダウンロードできます。
*クローズドな会ですので、ご参加には「成体脳のニューロン新生懇談会」への入会(入会金・年会費無料)が必要です。入会手続きは簡単ですので、お気軽に事務局にお問い合わせください。
参加費:1000円
意見交換会(18:30〜):サクラサイドテラス(キャンパス内)
(学部生:1000円, 大学院生:2000円, それ以外:4000円)
担当幹事:名古屋市立大学大学院医学研究科再生医学分野 澤本和延
事務局:名古屋市立大学大学院医学研究科再生医学分野 金子奈穂子・澤田雅人
連絡先:naokoka@med.nagoya-cu.ac.jp
当研究室では、平成26年度より、日本学術振興会二国間交流事業として、スペインとの共同研究「神経再生過程の細胞間相互作用:最先端電子・光学顕微鏡イメージングを用いた共同研究」を行っています。本研究のため、当研究室のメンバー6名がバレンシア大学を訪問しました。
今年度より、愛知県・公益財団法人科学技術交流財団のご支援により、神経再生イメージング技術開発研究会 が発足しました。
再生医学をはじめ、医学・生物学研究において、細胞・組織をできる限り生体内に近い状態で培養しながら長期間観察する実験の重要性が高まっています。本研究会では、独自の高度な技術を有する近隣の企業等の方々にご参加いただき、再生器官の長期ライブイメージングを可能にする灌流システムの構築を目指した調査・検討を行うとともに、再生医学だけでなく、発生生物学や神経科学など様々な医学・生物学の分野における本システムの展開可能性の検討を行う予定です。
日本麻酔科学会第62回学術集会において、藤掛数馬・大学院生(麻酔科学・集中治療医学分野)が最優秀演題賞を受賞しました。



松本真実さん(写真中央)が大学院修士課程を修了し、4月から博士課程へ進学します。おめでとうございます。
(写真右は荻野君、左は小俣君で、お二人とも4月から修士課程2年生です。)
インターフェロンによるうつ病のメカニズムと対策についての新しい論文が掲載されました。昨年我々は、インターフェロン投与によって海馬のニューロン新生が抑制されうつ病を発症するメカニズムを発表しましたが、この論文では、これらの過程には脳内のミクログリアが関わっており、ミクログリア活性化を抑制する薬剤の投与によって改善できることを明らかにしました。
Zheng LS, Kaneko N# and Sawamoto K# (#corresponding authors)
Minocycline treatment ameliorates interferon-alpha-induced neurogenic defects and depression-like behaviors in mice
Front Cell Neurosci 9:5 (2015)
名古屋市立桜台高等学校より、再生医学に興味を持つ生徒さん達と先生が当研究室を訪問しました。研究室のメンバーと一緒に、脳の解析や結果の発表、ディスカッションをしました。
桜台高校のホームページにも掲載されています。
太田晴子助教(麻酔・危機管理医学)が2014年度名古屋市立大学医学会賞を受賞しました。

匹田貴夫元助教(現在マックスプランク研究所)が、Journal of Neurochemistry誌よりMark A. Smith Prize を受賞しました。この賞は、毎年35歳以下の研究者がfirst authorまたはlast authorとして発表した論文のうち、最も優れたものをEditorが選んで贈呈するものです。
Rac1-mediated indentation of resting neurons promotes the chain migration of new neurons in the rostral migratory stream of post-natal mouse brain J Neurochem 128(6), 790-797. Takao Hikita, Akihisa Ohno, Masato Sawada, Haruko Ota and Kazunobu Sawamoto. DOI: 10.1111/jnc.12518
“The winning paper sheds light on cell migration mechanisms using cutting edge techniques such as live cell imaging, and thus has broad appeal and impact in the neurochemistry and neuroscience fields.”
脳内で幹細胞から作られる新生ニューロンが、速度調節をしながら移動する仕組みに関する論文がNature Communicationsに掲載されました。
Ota H#, Hikita T#, Sawada M#, Nishioka T, Matsumoto M, Komura M, Ohno A, Kamiya Y, Miyamoto T, Asai N, Enomoto A, Takahashi M, Kaibuchi K, Sobue K, Sawamoto K [#co-first authors]
Speed control for neuronal migration in the postnatal brain by Gmip-mediated local inactivation of RhoA
Nat Commun 5: 4532 (2014)
今回の研究により、ニューロンの中でGmipという蛋白質が作用することで、ブレーキが働いて移動速度を調節し、脳内の適切な場所に停止させる仕組みの一端が解明されました。
DOI: 10.1038/ncomms5532 Pubmed
筆頭著者による研究内容の解説はこちら
バイオマテリアルを用いて「足場」を整えることにより、傷害を受けた脳組織へのニューロンの移動を促進する技術についての研究成果が、Tissue Engineering Part A誌に掲載されました。
Ajioka I#, Jinnou H#, Okada K, Sawada M, Saitoh S, Sawamoto K [#Co-first authors]
Enhancement of neuroblast migration into the injured cerebral cortex using laminin-containing porous sponge
Tissue Eng Part A 21: 193-201(2015)
(Online instant publication of accepted manuscript)
我々は以前、脳室下帯で産生される新生ニューロンが血管を足場として傷害後の脳組織を移動することを見いだしました。本研究では、血管周囲に豊富に存在する細胞外マトリックス蛋白質であるLamininを含有するスポンジ状のマテリアルを作製し、人工的な足場を脳内に整備することにより、脳室下帯から傷害を受けた大脳皮質へ新生ニューロンを誘導することに成功しました。東京医科歯科大学・味岡先生らとの共同研究です。
筆頭著者による研究内容の解説はこちら
成体海馬におけるニューロン新生とうつ病に関する研究の成果が、Stem Cell Reports誌に掲載されました。
インターフェロンが中枢神経系のインターフェロン受容体を介して海馬におけるニューロン新生の低下と抑うつ症状を引き起こすことを明らかにしました。
本研究は、厚生労働省肝炎等克服緊急対策研究事業などのサポートによって行われました。
Zheng LS,* Hitoshi S,* Kaneko N,*# Takao K, Miyakawa T, Tanaka Y, Xia H, Kalinke U, Kudo K, Kanba S, Ikenaka K, Sawamoto K# [*co-first authors; #corresponding authors]
Mechanisms for interferon-alpha-induced depression and neural stem cell dysfunction
Stem Cell Rep 3: 73-84 (2014)
http://dx.doi.org/10.1016/j.stemcr.2014.05.015
筆頭著者による研究内容の解説はこちら
現在、2015年4月より研究に参加する大学院生(博士課程・修士課程)を募集しています。
ご興味のある方は、お気軽にメールで連絡して下さい(澤本和延 sawamoto@med.nagoya-cu.ac.jp)。
分子・細胞・個体レベル(マウス・サル・ゼブラフィッシュ)の様々な手法を用いています。
現在の主な研究内容
・成体脳室下帯におけるニューロン新生・細胞移動
・脳疾患モデルを用いたニューロン・グリアの再生機構解明と再生誘導方法の開発
・ニューロン新生における血管の役割
・嗅覚とニューロン新生の関係
・うつ病と海馬のニューロン新生の関係
・上衣細胞の繊毛の極性のメカニズムと意義
・神経幹細胞の老化のメカニズムと対策
(入試関係のスケジュールや過去問などの情報については本学のホームページに掲載されております。)
フランスの共同研究者が3名来訪し、当研究室のメンバーと交流しました。これは日仏両政府の支援により国際交流を促進するためのプログラムの活動として行っているものです。
名古屋市立大学によるプレスリリース
本学医学研究科再生医学分野の澤本和延教授と岸本憲人特任助教らの研究グル
ープは、魚を用いた研究によって、成体脳内の神経回路の左右差を作り出す
仕組みを解明しました。この成果は、米国の科学雑誌ネイチャー・ニューロサ
イエンスに掲載されます(米国東部時間5 月19 日午後2 時)。
私たちの脳は左脳と右脳に分かれていて、それぞれの構造や役割に違いがあ
ることが知られています。これらの脳の左右差は、子供から大人に成長するに
つれてよりはっきりとしてくることがわかっています。しかし、成長とともに
右脳と左脳の違いを作り出す遺伝子についてはあまり良くわかっていません。
今回の研究では、ゼブラフィッシュという小型淡水魚を用いた実験によって、
成体期の脳内に存在する神経幹細胞から新しく生まれる細胞の運命を決める
Myt1 という遺伝子が右脳よりも左脳で強く働くことにより、嗅覚の左右差を作
り出している仕組みを初めて明らかにしました。
この仕組は、ヒトの脳の左右差の解明に役立つ可能性があります。
本研究は、本学の他、国立遺伝学研究所、トゥールーズ大学(仏国)が参加
した国際共同研究です。
<内容の詳細>
研究背景
私たちの体は一見左右対称ですが、利き手、利き足、利き目、利き耳があることから もわかるように、左右一対の身体(器官)のうちどちらか片側を好んで使用しています。 これは、成長とともに右脳と左脳に違いが生じ、特定の機能においては片側の脳の神経 回路が優位に働くようになるためと考えられます。これまでの研究によって、左脳・右 脳が機能分業することによって効率的な情報処理を行うことがわかってきましたが、左 右差を生み出す遺伝子や、その意義については十分に研究されていませんでした。そこ で、私たちは、遺伝子工学的な実験に適した小型淡水魚であるゼブラフィッシュ(学名: Danio rerio)を用いて、成体期において脳神経回路の左右差を作り出しているメカニズ ムを調べました。 研究成果 私たちは、ゼブラフィッシュの脳内で働いている多数の遺伝子を「遺伝子トラップ法」 という方法を使って、緑色蛍光タンパク質(GFP)で標識して観察しました。その結果、 幹細胞から作られる新しい神経細胞の運命を決定するMyt1 という遺伝子の働きが、成 長にともなって変化し、左脳の中の嗅覚に関係する部分で優位になるということを発見 しました。この遺伝子を持たない魚では、普通の魚よりも嗅覚が劣っているこ とから、Myt1 が嗅覚に必須な遺伝子であることもわかりました。 魚に利き鼻があるのかどうかを調べるために、成魚の片側の鼻に栓をして、好きな匂 い(アミノ酸)へ向かって泳ぐ行動(誘引行動)を調べました。右鼻に栓をしても誘引 行動には影響がありませんが、左鼻に栓を挿入するとアミノ酸への誘引行動ができなく なったことから、左鼻が利き鼻であることがわかりました。さらに、左鼻に栓 をしてから1週間経過すると、Myt1 が右側で強く働くようになり、アミノ酸への誘引 行動ができようになりました。このことから、魚は、利き鼻の機能を失った場 合に、脳内の遺伝子の働きを変化させて反対側の鼻を利き鼻に替えることができるとい うことがわかりました。 これらの実験によって、Myt1 が左脳で強く働くことによって、新しい神経細胞の産 生が左右非対称となり、魚の利き鼻が作られていることがわかりました。 成果の意義 この研究は、成体期につくられる嗅覚に関わる神経細胞の右脳と左脳における違いを 作り出す遺伝子を明らかにし、その嗅覚における意義を示したものです。脳細胞は生ま れた時にほぼ完成していて、年齢とともに適応能力が低下していくと考えられています が、この研究の結果から、成体になっても嗅覚に関わる部位に新しい脳細胞が付け加わ ることによって、右脳と左脳が持つ役割が変化することがわかりました。また、ヒトと ゼブラフィッシュではゲノムや脳の構造が似ていることから、ヒトの脳内における神経 回路の左右非対称性にも同様のメカニズムが関わっている可能性もあります。したがっ て、本研究の成果は、ヒトの脳の構造と機能の左右差の解明にも役立つことが期待され ます。

今後の展開
本研究で用いた遺伝子トラップ法を大規模に行うことで、脳内の様々な神経回路で左 右非対称な働きをしている遺伝子の探索が可能になります。これによって、例えば、左 脳に言語野を作り出すメカニズムなど、未だ不明な点の多い脳の左右差形成の仕組みの 解明に役立つことが期待できます。
<掲載される論文の詳細>
掲載誌:Nature Neuroscience 電子版
題目:Interhemispheric asymmetry of olfactory input-dependent neuronal specification in the adult brain
著者:岸本憲人(名古屋市立大学)、浅川和秀(国立遺伝学研究所)、Romain Madelaine (トゥールーズ大学)、Patrick Blader (トゥールーズ大学)、川上浩一(国立遺伝学研究 所)、澤本和延(名古屋市立大学)
以 上
以下の募集は終了しました。多数のご応募ありがとうございました。
|
仕事内容 |
マウスの行動解析、脳の組織解析、遺伝子改変マウスの繁殖管理、遺伝子タイピングなど。詳細はお問い合わせください。 |
|
雇用期間 |
平成25年4月以降平成26年3月31日まで ※1年ごとの更新 |
|
勤務地 |
名古屋市瑞穂区瑞穂町字川澄1番地 名古屋市立大学大学院医学研究科 再生医学分野 |
|
給与等 |
時給:1027〜1380円(経験、または資格に応じて名市大職員規程に準じ処遇します。) ※応募資格:理系の大学、短大、専門学校卒、動物アレルギーのない方。未経験の方も指導いたします。 |
|
交通費 |
別途支給、1日460円まで |
|
社会保険等 |
健康保険・雇用保険・厚生年金保険・労災保険に加入
|
|
勤務日 |
月曜〜金曜のうち4〜5日(国民の祝日は除く)※応相談 ※有給休暇あり |
|
勤務時間 |
午前9時00分〜午後5時00分まで(休憩1時間)勤務日数、勤務時間については相談可 |
|
募集人員 |
1名 |
|
応募方法 |
面接選考を行いますので、下記連絡先まで履歴書(書式自由)を郵送にて送付ください。3月13日(水)必着(面接の日時は追ってご連絡致します。)但し、期間中でも採用者が決定次第終了。 |
|
問い合わせ・担当者 |
〒467-8601 名古屋市瑞穂区瑞穂町字川澄1番地名古屋市立大学大学院医学研究科 再生医学分野
担当:筧(かけい) 理恵 電話:052-853-8532 e-mail:rie_k@med.nagoya-cu.ac.jp |
名古屋市立大学によるプレスリリース
本学医学研究科の澤本和延教授(再生医学)と加古英介助教(麻酔・危機管理医学)らの研究グループは、新生児脳の白質傷害モデルマウスを使った実験により、オリゴデンドロサイトという脳の細胞の再生を促進することに成功しました。この成果は、米国の科学雑誌ステムセルズに掲載されます(米国東部時間8月13日)。
新生児期の脳では、血流や酸素供給が不足すると、神経の繊維が集まっている白質と呼ばれる部分が傷害を受けて、小児麻痺や痙攣などを引き起こすことが知られています。現在、この病気が起こったあとに有効な治療法は知られていません。今回の研究では、特殊なマウスを用いて、白質が傷害を受けた時のオリゴデンドロサイトという細胞の再生のしくみを明らかにしました。さらに、アシアロエリスロポエチンというたんぱく質を投与することで、脳内に存在する幹細胞からつくられる新しいオリゴデンドロサイトの成熟・再生を促進し、歩行機能を改善させることに成功しました。
この方法は、脳室周囲白質軟化症などの新生児白質傷害に対する再生医療に役立つ可能性があります。
本研究は、本学と生理学研究所(愛知県岡崎市)の共同研究として行われました。
<内容の詳細>
背景
近年の研究により、脳内の「脳室」と呼ばれる部分の近くに幹細胞が存在し、脳の細胞を再生していることが明らかになってきました。また、こうした幹細胞の再生能力は、大人よりも子どもの方が高いことが知られています。しかし、新生児に一旦、白質傷害とよばれる脳傷害が起こってしまうとその後の再生が十分に起こらず、麻痺・痙攣等の症状が一生残ってしまうことが多く、その理由は不明でした。
このような疾患において、白質を通る神経の繊維を取り囲み神経の情報伝達において重要な役割を果たしている「オリゴデンドロサイト」という細胞が傷害を受けやすいことが知られていました。従って、オリゴデンドロサイトを再生させることができれば、白質傷害の治療に役立つと考えられます。本研究では、脳室の近くに存在する未熟なオリゴデンドロサイトから白質組織が再生されるしくみを詳しく調べ、マウスに薬剤を投与して再生を促進することができるかを調べました。
?研究手法
生後5日のマウスに対して、脳を流れる血液を減少させる手術を行い、酸素が薄い環境で飼育することによって、新生児白質傷害の動物モデルを作製しました。オリゴデンドロサイトだけが光る遺伝子改変マウスを用いて、傷害後に未熟なオリゴデンドロサイトがどのように白質を形成するかを調べました。その結果、脳室の周りや傷害された白質において、多くの未熟なオリゴデンドロサイトが増殖しているのにも関わらず、時間がたってもその大部分が正常な細胞に成熟できないことを発見しました。従って、これらの未熟なオリゴデンドロサイトを成熟させることができれば、白質の再生を促進することができると考えられます。
そこで、未熟なオリゴデンドロサイトの成熟を促進するために、細胞成熟効果を持つアシアロエリスロポエチンというタンパク質をマウスに投与しました。傷害が起こり始めた後にアシアロエリスロポエチンを投与し、脳の細胞を顕微鏡で解析したところ、治療を開始したマウスでは徐々に細胞の成熟が促進されて、2週間後には正常な部分と同程度まで改善することがわかりました(図)。さらに成体マウスとなった時点で脳の構造や機能を解析したところ、アシアロエリスロポエチンで治療したマウスでは白質組織の再生が促進されており、歩行機能も正常近くまで改善していました。
結論
新生児における白質傷害の後の脳において、脳室の周囲で生まれたオリゴデンドロサイトが未熟なままとどまっていることを明らかにしました。さらに、アシアロエリスロポエチンを投与することによって、これらの細胞を成熟させて、白質の再生を促進することに成功しました。
医療への応用の可能性
今回使用したアシアロエリスロポエチンは、貧血などの患者によく使われるエリスロポエチンの構造を変化させた薬剤であり、人体に対する安全性が高いと考えられています。また、今回の実験結果は、脳にダメージが起こって数日後に投与を開始しても脳組織を再生できるという可能性を示しており、現在治療法がない脳疾患の再生医療に役立つ可能性があります。
?<掲載される論文の詳細>
題名:Subventricular zone-derived oligodendrogenesis in injured neonatal white-matter in mice enhanced by a nonerythropoietic EPO derivative.
著者:加古英介(名古屋市立大)、金子奈穂子(名古屋市立大)、青山峰芳(名古屋市立大学)、飛田秀樹(名古屋市立大)、竹林浩秀(生理学研究所)、池中一裕(生理学研究所)、浅井清文(名古屋市立大学)、戸苅創(名古屋市立大)、祖父江和哉(名古屋市立大学)、澤本和延(名古屋市立大)
?
名古屋市立大学によるプレスリリース
脳内における神経細胞の再生のしくみに関する研究成果の発表について
本学医学研究科の澤本和延教授(再生医学)と同大学院生澤田雅人らの研究グループは、脳内で神経細胞が入れ替わる再生のしくみを解明しました。この成果は、米国の科学雑誌ジャーナル・オブ・ニューロサイエンスに掲載されます(米国東部時間8月10日)。
近年、成人の脳の中にも幹細胞が存在し、新しい神経細胞がつくられていることがわかってきました。しかし、古くなったり病気によって死んだりした神経細胞がどのようにして新しい神経細胞と入れ替わっているかは不明でした。今回の研究では、特殊な顕微鏡を用いて、生きた動物の脳内の神経細胞を長期間観察し続けることにより、神経細胞が死んだ場所に新しい神経細胞が加わるしくみがあること、そして、このしくみが脳の活動によって調節されていることが初めて解明されました。
このしくみは、例えば脳疾患を再生医療によって治療する方法の開発に役立つ可能性があります。
本研究は、本学及び生理学研究所(生体恒常機能発達機構研究部門)等が参加した共同研究として行われました。
<内容の詳細>
背景
近年の研究により、成人の脳にも幹細胞が存在して、神経細胞を再生していることが明らかになってきました。これまでの研究方法では、死後脳を解析していたため、脳内でどのように神経細胞が入れ替わり、再生されるのかは不明でした。また、神経細胞の再生と脳の活動の関係については、ほとんどわかっていませんでした。今回我々は、生きた動物で神経細胞を長期間観察する技術を使って、神経細胞の再生のしくみと脳の活動の関係について詳しく調べました。
研究手法
脳内で匂いの情報処理に関わる嗅球と呼ばれる部位では、活発に神経細胞が再生することが知られています。今回我々は、生理学研究所鍋倉淳一教授らとの共同研究によって、生きたまま脳の中の神経細胞を観察することができる「二光子顕微鏡」という特殊な顕微鏡を使い、嗅球の神経細胞を2ヶ月にわたって繰り返し観察し続けました。その結果、古い神経細胞が死んだり、新しい神経細胞が神経回路に加わったりする様子を捉えることに成功しました。また、レーザーを用いて狙った神経細胞を殺すと、同じ場所に新しい神経細胞が再生されることを見出しました。さらに、マウスの鼻に栓を挿入して匂いの情報を遮断し、脳への刺激を失わせると、同じ場所での神経細胞の再生は起こらなくなることが分かりました。
結論
脳内で神経細胞が死んだ場所に新しい神経細胞が加わるしくみが存在し、そのしくみは脳の活動によって調節されていることが初めて解明されました。
医療への応用の可能性
我々のこれまでの研究により、脳内の幹細胞から産生される新しい神経細胞は、脳梗塞等の疾患で多くの神経細胞が死滅すると、その領域へと移動し、神経細胞の一部を再生することがわかってきました。しかし、その再生効率が低いため、脳の機能は十分に回復しません。今回明らかになったしくみを応用して失われた神経細胞の再生効率を高めることができれば、脳疾患の治療に役立つ可能性があります。また、脳の活動によって新しい神経細胞が加わるしくみを解明することで、傷害後のリハビリテーション法の向上や、iPS細胞などを用いた再生医療に貢献する可能性があります。
<掲載される論文の詳細>
掲載誌:Journal of Neuroscience、第31巻、11587−11596ページ
題名:Sensory input regulates spatial and subtype-specific patterns of neuronal turnover in the adult olfactory bulb
著者:澤田雅人(名古屋市立大)、金子奈穂子(名古屋市立大)、稲田浩之(生理学研究所)、和氣弘明(生理学研究所)、加藤康子(名古屋市立大)、柳川右千夫(群馬大)、小林和人(福島医科大)、根本知己(北海道大)、鍋倉淳一(生理学研究所)、澤本和延(名古屋市立大)
現在、平成24年4月より研究に参加する大学院生(博士課程・修士課程)を募集しています。
ご興味のある方は、お気軽にメールで連絡して下さい(澤本和延 sawamoto@med.nagoya-cu.ac.jp)。
分子・細胞・個体レベル(マウス・サル・ゼブラフィッシュ)の様々な手法を用いています。
医学・理学・理工学・薬学・農学部出身者を含む多様なメンバー構成になっております。
現在の研究内容
・成体脳室下帯におけるニューロン新生・細胞移動
・脳室壁の繊毛運動と液流の発生のメカニズム
・嗅覚とニューロン新生の関係
・虚血性脳疾患モデルを用いたニューロン・グリアの再生機構解明と再生誘導方法の開発
・インターフェロン療法におけるうつ病と海馬のニューロン新生
(入試関係のスケジュールや過去問などの情報については本学のホームページに掲載されております。)
実験補助員の募集は終了しました。
***********************
実験補助員を1名募集いたします。
名古屋市立大学大学院医学研究科再生医学分野では、損傷後の脳内でニューロンを再生することを目指した分子・細胞・個体レベルの様々な研究を行っています。この度、マウスを用いた実験の補助をして下さる方を募集します。
仕事内容:マウス脳の組織解析、遺伝子改変マウスの繁殖管理、遺伝子タイピングなど。詳細はお問い合わせください。
待遇:非常勤/名古屋市立大学の規定によります。
勤務時間: 9:00-17:00(休憩1時間を含む):応相談
休日:土、日、祝日および年末年始、有給休暇あり
給料:時間給1027〜1380円
通勤手当:1日460円を限度に支給
保険:健康保険、厚生年金保険、労災、雇用保険
勤務地:名古屋市立大学大学院医学研究科再生医学分野
URL:http://k-sawamoto.tk/
募集期間:2011年5月31日(火)まで。
適任者が決定し次第、募集を終了します。
選考内容:書類選考後、面接を行います。
着任時期:採用決定後のできるだけ早い時期(応相談)。
応募資格:理系の大学、短大、専門学校卒、動物アレルギーのない方。
未経験の方も指導いたします。
応募方法:下記まで、履歴書をお送り下さい(eメール可)。メールでのお問い合わせも受け付けます。
[連絡先]〒467-860名古屋市瑞穂区瑞穂町字川澄1
名古屋市立大学大学院医学研究科 再生医学分野
金子 奈穂子 naokoka@med.nagoya-cu.ac.jp
Tel(052)853-8532
新生ニューロンがアストロサイトにトンネルを形成させながら移動するメカニズムに関する研究の成果が、Neuron誌に掲載されました。
Kaneko N, Marin O, Koike M, Hirota Y, Uchiyama Y, Wu JY, Lu Q, Tessier-Lavigne M, Alvarez-Buylla A, Okano H, Rubenstein JL, Sawamoto K
New Neurons Clear the Path of Astrocytic Processes for Their Rapid Migration in the Adult Brain.
Neuron 67:213-223 (2010)
筆頭著者による研究内容の解説はこちら
Featured Article
New Neurons Clear the Path of Astrocytic Processes for Their Rapid Migration in the Adult Brain.
Kaneko N, Marín O, Koike M, Hirota Y, Uchiyama Y, Wu JY, Lu Q, Tessier-Lavigne M, Alvarez-Buylla A, Okano H, Rubenstein JL, Sawamoto K.
FULL TEXT Neuron. 2010 Jul 29;67(2):213-223.
PREVIEW in Neuron:?Going Tubular in the Rostral Migratory Stream: Neurons Remodel Astrocyte Tubes to Promote Directional Migration in the Adult Brain
Research Highlights in Nature:Tunnelling brain cells
Research Highlights in Nature Reviews Neuroscience: Neuron-Glia Interactions A tunnel signal
名古屋市立大学によるプレスリリース
名古屋市立大学医学研究科・澤本和延教授と金子奈穂子助教らの研究グループ(再生医学)は、脳内でつくられる新しい神経細胞が長距離を高速度で移動するしくみを解明しました。この成果は、米国の科学雑誌Neuronに掲載されます。
近年、大人の脳の中にも幹細胞が存在し、新しい神経細胞がつくられていることがわかってきました。そのような神経細胞が脳で働くためには、つくられた場所から遠く離れた場所へ移動しなければなりません。たくさんの細胞が密集している脳の中を、どのようにして神経細胞が移動するのかは、これまで不明でした。今回の研究により、新しい神経細胞が周囲の細胞を押し分けてトンネル状の通り道をつくるしくみによって、長距離を高速度で移動できることが初めて解明されました。
このしくみは、例えば脳梗塞や脳室周囲白質軟化症などの脳疾患を再生医療によって治療する方法の開発に役立つ可能性があります。
本研究は、本学の他、順天堂大学、慶應義塾大学、ミグエルヘルナンデス大学(スペイン)、ノースウエスタン大学(米国)、シティオブホープ医学研究所(米国)、カリフォルニア大学サンフランシスコ校(米国)、ジェネンテック社(米国)が参加した国際共同研究です。
背景:近年の研究により、成人の脳にも幹細胞が存在して、新しい神経細胞(ニューロン)をつくり続けていることが明らかになってきました。脳の内部にある側脳室の壁に沿って存在する「脳室下帯」と呼ばれる部分は、脳内で最も活発にニューロンがつくられている場所です。この脳室下帯でつくられた神経細胞は、脳の前方まで長距離を移動して、嗅覚に関連したさまざまな機能を担う細胞へと成熟します。また脳梗塞などの疾患によってたくさんの脳細胞が死滅すると、傷害を受けた部位に移動してニューロンの一部を再生します。しかし、脳は細胞や線維が密集した組織であり、これらのニューロンがその中をどのようにして遠くまで移動しているのか、そのしくみは分かっていませんでした。今回我々は、ニューロンがアストロサイトという別の種類の細胞がつくるトンネルの中を通ることに着目して、そのしくみを詳しく調べました。
研究手法:細胞移動の調節に関わるSLITタンパク質をコードする遺伝子を欠失したマウスの脳を解析したところ、脳室下帯からのニューロンの移動速度が低下し、トンネルを形成するアストロサイトの形が不規則になっていることがわかりました。SLITタンパク質の受容体であるROBOの分布を調べたところ、トンネルを形成しているアストロサイトに局在していました。様々な培養法を使って、細胞の形の変化や移動する様子を詳細に解析したところ、ニューロンが分泌するSLITがアストロサイトの表面に存在するROBOに結合すると、アストロサイトが引っ込んで脳内にトンネル構造がつくられることがわかりました。
結論:移動するニューロンがSLITタンパク質を分泌することにより周囲のアストロサイトに働きかけ、自らの高速移動のためのトンネルの整備を行うという新しいメカニズムが明らかになりました。
医療への応用の可能性:脳内におけるニューロンの移動をコントロールして目的の部位に効率よく到達させることが可能になれば、現在は治療の難しい脳の病気、例えば脳梗塞や脳室周囲白質軟化症・神経変性疾患などを、私たち自身が持っている再生能力を活用し「再生医療」によって治療する方法の開発に役立つ可能性があります。また、iPS細胞を使って作成した神経細胞を移植する再生医療においても、移植後の細胞の移動をコントロールすることが重要と考えられます。
Kojima T, Hirota Y, Ema M, Takahashi S, Miyoshi I, Okano H, Sawamoto K
Subventricular zone-derived neural progenitor cells migrate along a blood vessel scaffold toward the post-stroke striatum.
Stem Cells 28:545-554 (2010)
Subventricular Zone-Derived Neural Progenitor Cells Migrate Along a Blood Vessel Scaffold Toward the Post-Stroke Striatum
Kojima T, Hirota Y, Ema M, Takahashi S, Miyoshi I, Okano H, Sawamoto K.
The subventricular zone (SVZ) of the adult brain contains neural stem cells that have the capacity to regenerate new neurons after various insults. Brain ischemia causes damage to brain tissue and induces neural regeneration together with angiogenesis. We previously reported that, after ischemic injury in mice, SVZ-derived neural progenitor cells (NPCs) migrate into the striatum, and these NPCs are frequently associated with blood vessels in the regenerating brain tissue. Here we studied the role of blood vessels during the neural regeneration in more detail. BrdU administration experiments revealed that newly generated NPCs were associated with both newly formed and pre-existing blood vessels in the ischemic striatum, suggesting that the angiogenic environment is not essential for the neuron-blood-vessel interaction. To observe migrating NPCs and blood vessels simultaneously in damaged brain tissue, we performed live imaging of cultured brain slices after ischemic injury. In this system, we virally labeled SVZ-derived NPCs in Flk1-EGFP knock-in mice, in which the blood vessels are labeled with EGFP. Our results provide direct evidence that SVZ-derived NPCs migrate along blood vessels from the SVZ toward the ischemic region of the striatum. The leading process of the migrating NPCs was closely associated with blood vessels, suggesting that this interaction provides directional guidance to the NPCs. These findings suggest that blood vessels play an important role as a scaffold for NPCs migration toward the damaged brain region.
Stem Cells 2010 Jan 13. [Epub ahead of print]
研究員募集は終了しました。
尚、平成22年度より本学大学院医学研究科(博士課程・修士課程)に入学し当研究室に参加することを検討されている方は、事前に澤本 (sawamoto@med.nagoya-cu.ac.jp) までご連絡下さい。
入試についてお知りになりたい方は、本学医学研究科ホームページをご覧下さい。
以下の募集は終了しました。
?
===========
当研究室では、現在以下の人材を募集しています。
1)ポスドク1名
成体脳内の海馬・脳室下帯に存在する神経幹細胞・前駆細胞の機能変化と抑うつ症状の関連についての研究に取り組むポスドクを1名募集します。実験内容としては、マウス脳の組織学的解析・初代培養細胞を用いた培養実験が主体となります。
資格:博士の学位を有するもの
着任時期:2009年6月〜(多少の変更は可能です。)
任期:2011年3月まで。成果により数年延長の可能性あり。
応募方法:履歴書(写真付き)・業績リスト(様式自由)・照会者連絡先(1名以上)をメールで下記問い合わせ先にお送りください。
締切:4月28日
締切後直ちに最終候補者に面接を受けて頂き、2週間以内に決定する予定です。
問い合わせ先:名古屋市立大学大学院医学研究科再生医学分野
金子奈穂子(naokoka@med.nagoya-cu.ac.jp)
アダルト神経新生と病態における変化に関する総説論文がNeuroscience Research誌に掲載されました。
Kaneko N, Sawamoto K
Adult neurogenesis and its alteration under pathological conditions.
Neurosci Res 63:155-164 (2009)

表紙のイラスト:マウス成体脳室下帯におけるニューロンの産生
脳室下帯の神経幹細胞(青)が産生するニューロン(赤)は嗅球へ移動して成熟する。
Kaneko, N and Sawamoto, K. (2009)
Adult neurogenesis and its alteration under pathological conditions
Neurosci. Res. 63: 155-164. (REVIEW ARTICLE)
【博士課程・修士課程の大学院生として研究に参加できます。】
学位論文のテーマとしては、例えば以下のような課題があります。
・げっ歯類・霊長類の成体脳室下帯におけるニューロン新生・移動メカニズムの解析
・感覚入力による成体嗅球ニューロン産生の制御機構の解析
・脳室上衣細胞の成熟と繊毛運動による液流発生のメカニズムと意義の解明
・ゼブラフィッシュの遺伝学的手法を用いたニューロン新生メカニズムの解明
・虚血性疾患モデルにおける神経再生メカニズムの解明と治療法の開発
問いあわせ:sawamoto@med.nagoya-cu.ac.jpまで。研究室見学も可能です。
【以下のポスドク募集は終了しました。多数のご応募ありがとうございました。】
ニューロンおよびグリア細胞の産生・移動・再生のメカニズムの研究に取り組むポスドクを1名募集します。ご興味に応じて、疾患モデル動物を用いた再生医療研究や創薬研究にも参加していただきます。
応募方法:履歴書・業績リスト・照会可能な方のお名前と連絡先(e-mail)を添付書類としてsawamoto@med.nagoya-cu.ac.jpまでお送り下さい。
締切:10月14日。その後直ちに面接を行い、10月中に決定します。
応募資格:博士の学位を有する者(または取得見込み)
着任時期:2009年4月1日
その他:任期4年間まで。着任後の実績に応じて、1−2年後に教員(特任助教)としての採用も可能です。
問いあわせ:sawamoto@med.nagoya-cu.ac.jpまでメールでお願いします。
————————————
【博士課程・修士課程の大学院生としても研究に参加できます。】
学位論文のテーマとしては、例えば以下のような課題があります。
・げっ歯類・霊長類の成体脳の脳室下帯におけるニューロン新生・移動メカニズムの解明
・脳室上衣細胞の成熟と繊毛運動による液流発生
・ゼブラフィッシュの遺伝学的手法を用いたニューロン新生メカニズムの解明
・虚血性疾患モデルにおける神経再生メカニズムの解明と治療法の開発
問いあわせ:sawamoto@med.nagoya-cu.ac.jpまで。研究室見学も可能です。
平成21年度 再生医学分野 大学院修士・博士課程 大学院生募集
神経発生再生のメカニズムに関する分子細胞生物学的研究と、これらを脳疾患の再生医療に発展させるためのトランスレーショナルリサーチを行っています。
教室は、医学・理学・理工学・薬学・農学部出身者を含む多様なメンバー構成になっています。
研究内容に興味のある方・出願を希望される方はお気軽にご連絡ください。
(澤本和延 sawamoto@med.nagoya-cu.ac.jp)
研究内容
・げっ歯類・霊長類の成体脳の脳室下帯におけるニューロン新生・移動メカニズムの解明
・脳室上衣細胞の成熟と繊毛運動による液流発生
・ゼブラフィッシュの遺伝学的手法を用いたニューロン新生メカニズムの解明
・虚血性疾患モデルにおける神経再生メカニズムの解明と治療法の開発
参考文献
「成体脳室下帯で誕生し移動するニューロン」 蛋白質 核酸 酵素 vol.53, pp.863-869 (2008)
「成体脳のニューロン新生とその異常」 BRAIN & NERVE vol.60, pp.319-328 (2008)
2007年11月30日に福岡市で開催された第15回日本血管医学生物学会学術大会において、大学院生の小島拓郎君が以下の内容で発表を行い、学会ポスター賞を受賞しました。
「神経再生過程の新生ニューロンの移動における血管の役割」
小島拓郎・廣田ゆき・山下徹・二宮充喜子・岡野栄之・澤本和延

生後脳の新生ニューロンの移動に関する研究の成果がThe Jpurnal of Neuroscienceに掲載されました。
Hirota Y, Ohshima T, Kaneko N, Ikeda M, Iwasato T, Kulkarni AB, Mikoshiba K, Okano H, Sawamoto K
Cyclin-dependent kinase 5 is required for control of neuroblast migration in the postnatal subventricular zone.
J Neurosci 27:12829-12838 (2007)
The Journal of Neuroscience, November 21, 2007, 27(47):12829-12838
Cyclin-Dependent Kinase 5 Is Required for Control of Neuroblast Migration in the Postnatal Subventricular Zone
Yuki Hirota, Toshio Ohshima, Naoko Kaneko, Makiko Ikeda, Takuji Iwasato, Ashok B. Kulkarni, Katsuhiko Mikoshiba, Hideyuki Okano, and Kazunobu Sawamoto
At the lateral wall of the lateral ventricles in the adult rodent brain, neuroblasts form an extensive network of elongated cell aggregates called chains in the subventricular zone and migrate toward the olfactory bulb. The molecular mechanisms regulating this migration of neuroblasts are essentially unknown. Here, we report a novel role for cyclin-dependent kinase 5 (Cdk5), a neuronal protein kinase, in this process. Using in vitro and in vivo conditional knock-out experiments, we found that Cdk5 deletion impaired the chain formation, speed, directionality, and leading process extension of the neuroblasts in a cell-autonomous manner. These findings suggest that Cdk5 plays an important role in neuroblast migration in the postnatal subventricular zone.
Key words: Cdk5; neuroblast; migration; subventricular zone; rostral migratory stream; postnatal neurogenesis
成体神経前駆細胞の増殖シグナルに関する研究の成果がStem Cells Jpurnalsに掲載されました。
Adachi K, Mirzadeh Z, Sakaguchi M, Yamashita T, Nikolcheva T, Gotoh Y, Peltz G, Gong L, Kawase T, Alvarez-Buylla A, Okano H, Sawamoto K
Beta-catenin signaling promotes proliferation of progenitor cells in the adult mouse subventricular zone.
Stem Cells 25:2827-2836 (2007)
筆頭著者による研究内容の解説はこちら
Stem Cells. 2007 Aug 2; PMID: 17673525
β-catenin signaling promotes proliferation of progenitor cells in the adult mouse subventricular zone
Kazuhide Adachi, Zaman Mirzadeh, Masanori Sakaguchi, Toru Yamashita, Tania Nikolcheva, Yukiko Gotoh, Gary Peltz, Leyi Gong, Takeshi Kawase, Arturo Alvarez-Buylla, Hideyuki Okano, Kazunobu Sawamoto
Abstract
The subventricular zone (SVZ) is the largest germinal zone in the mature rodent brain, and it continuously produces young neurons that migrate to the olfactory bulb. Neural stem cells in this region generate migratory neuroblasts via highly proliferative transit-amplifying cells. The Wnt/β-catenin signaling pathway partially regulates the proliferation and neuronal differentiation of neural progenitor cells in the embryonic brain. Here, we studied the role of beta-catenin signaling in the adult mouse SVZ. β-catenin-dependent expression of a destabilized form of green fluorescent protein was detected in progenitor cells in the adult SVZ of Axin2-d2EGFP reporter mice. Retrovirus-mediated expression of a stabilized β-catenin promoted the proliferation of Mash1+ cells and inhibited their differentiation into neuroblasts. Conversely, the expression of Dkk1, an inhibitor of Wnt signaling, reduced the proliferation of Mash1+ cells. In addition, an inhibitor of GSK3 promoted the proliferation of Mash1+ cells, and increased the number of new neurons in the olfactory bulb 14 days later. These results suggest that β-catenin signaling plays a role in the proliferation of progenitor cells in the SVZ of the adult mouse brain.
Key Words. β-catenin, neurogenesis, cell proliferation, subventricular zone, olfactory bulb, Mash1
私たちのグループは、5月1日より名古屋市立大学へ移転します。このサイトでは、新たに開設される「再生医学分野」のホームページとして、引き続き我々の活動の内容などを公開する予定です。しばらくお待ち下さい。
2007年2月24日午後1時より、本講座の公開研究報告会が慶應義塾大学信濃町キャンパスで行われる予定です。「第6回成体脳のニューロン新生懇談会」と合わせて開催されます。
1.スライド発表講演(1人15分)に加えて、ポスター発表のスペースを準備致します。
2.終了後、信濃町のお店で交流会を行います。
成体脳ニューロン新生懇談会会員以外の方にも自由にご参加いただけますが、会場等の都合上、参加を希望される方は、以下のアンケートにご回答頂き、メールにて澤本に(sawamoto@sc.itc.keio.ac.jp)ご連絡下さい。
++++++++++
お名前:
御所属:
懇談会に: ご出席 ご欠席
交流会に: ご出席 ご欠席
発表を: する しない
++++++++++
発表される場合には、下記の内容を記載したファイルを添付書類としてお送り下さい。
1)発表のタイトル
2)発表者氏名
3)発表者所属
4)要旨(500字程度)
5)発表形式希望(スライド または ポスター)
締切は2007年1月末日とさせていただきます。尚、スライド希望の方が多数いらっしゃる場合には、ポスターに変更をお願いする場合がございますので、予めご了承下さい。


















